 Das ist die Transkription einer Folge meines Sternengeschichten-Podcasts. Die Folge gibt es auch als MP3-Download und YouTube-Video. Und den ganzen Podcast findet ihr auch bei Spotify.
Das ist die Transkription einer Folge meines Sternengeschichten-Podcasts. Die Folge gibt es auch als MP3-Download und YouTube-Video. Und den ganzen Podcast findet ihr auch bei Spotify.
Mehr Informationen: [Podcast-Feed][iTunes][Bitlove][Facebook] [Twitter]
Über Bewertungen und Kommentare freue ich mich auf allen Kanälen.
—————————————————————————————
Sternengeschichten Folge 396: Technetium
In der heutigen Folge der Sternengeschichten wird es zuerst ein wenig chemisch aber dann sehr schnell sehr astronomisch. Denn es geht um das chemische Element Technetium. Von dem haben vermutlich die meisten noch nicht allzu viel gehört. Was einerseits nicht verwunderlich ist, andererseits aber auch sehr schade.
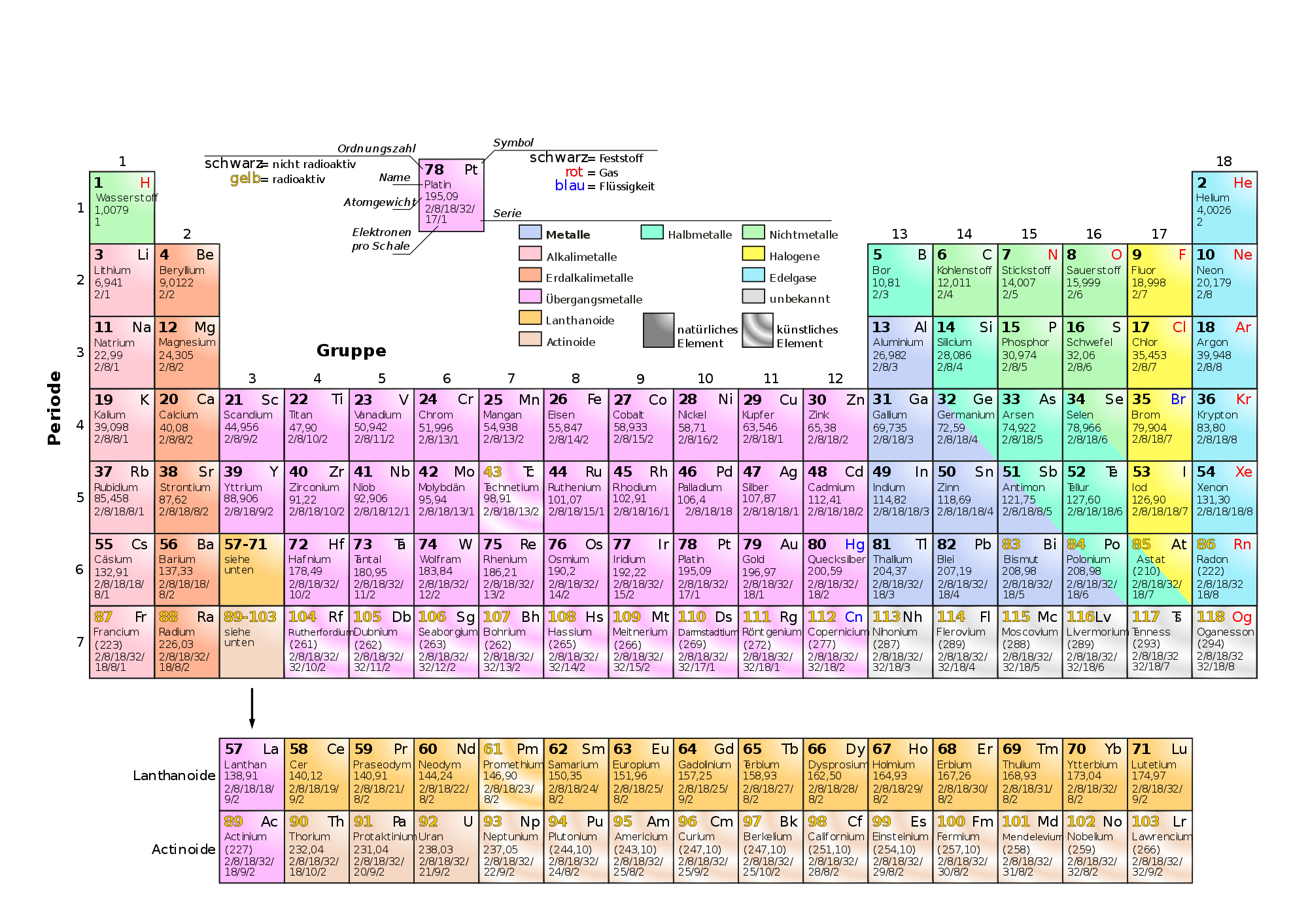
Technetium hat im Periodensystem der Elemente die Ordnungszahl 43. Und ist von Anfang an unangenehm aufgefallen. Es war nämlich nicht da. Als Dmitri Mendelejew im 19. Jahrhundert sein heute berühmtes System zur Ordnung der chemischen Elemente aufgestellt hat, war da von Anfang an eine Lücke. Man kannte das chemische Element mit der Ordnungszahl 42, nämlich Molybdän. Und man kannte das Element mit der Ordnungszahl 44, das ist Ruthenium. Nur Element Nummer 43 war nirgendwo zu finden. Es musste aber eigentlich da sein. Denn die Ordnungszahl ist ja nichts anderes als die Anzahl an Protonen, die der entsprechende Atomkern besitzt. Molybdän hat also 42 Protonen in seinem Atomkern; der Kern von Ruthenium ist aus 44 Protonen aufgebaut. Da muss es doch auch Atomkerne mit 43 Protonen geben. Und diverse Leute haben auch gemeint, sie hätten das fehlende Element entdeckt – hat sich aber immer als Fehlalarm herausgestellt. Ein echter Nachweis ist erst 1937 gelungen. Die beiden Wissenschaftler Emilio Segrè und Carlo Perrier von der Universität Palermo hatten sich anscheinend gedacht, dass sie das Element am besten selbst herstellen, wenn es sonst nirgendwo zu finden ist. Also nahmen sie eine dünne Molybdänfolie und schossen Wasserstoffatome drauf. Molybdän hat 42 Protonen, Wasserstoff hat ein Proton, zusammen gibt das 43 Protonen. Natürlich ist der genaue Prozess wesentlich komplizierter, die Atomkerne bleiben ja nicht einfach so aneinander kleben wie zwei Legosteine. Aber die Details ignorieren wir jetzt einfach und stellen fest, dass das fehlende Element durch dieses Experiment eindeutig hergestellt und nachgewiesen werden konnte. Segrè und Perrier gaben ihm den Namen Technetium, nach dem griechischen Wort für „künstlich“, weil es eben künstlich hergestellt werden musste.
Eine genaue Untersuchung des Elements zeigte dann auch, wieso es ansonsten nirgendwo zu finden war. Es war radioaktiv. Das heißt, es war nicht stabil: Der Kern eines radioaktiven Atoms kann nicht von selbst dauerhaft zusammenhalten; er zerfällt irgendwann spontan und wandelt sich dadurch in andere chemische Element um. Radioaktivität kannte man damals schon und auch radioaktive Elemente. Aber Technetium war außergewöhnlich. Viele Elemente sind radioaktiv, zum Beispiel der Kohlenstoff. Allerdings nicht der „normale“ Kohlenstoff, also der Kohlenstoff aus dem etwa wir Menschen zu einem großen Teil bestehen. Radioaktiv ist nur ein Isotop des Kohlenstoffs, also eine Variation des Atoms bei dem der Kern zwar die gleiche Anzahl an Protonen hat wie normaler Kohlenstoff, aber eine unterschiedliche Anzahl an Neutronen. Die sind ja die zweite Art von Atomkernbausteinen die es gibt und sie haben einen großen Einfluss auf die Stabilität des Atomkerns. Kohlenstoff hat 6 Protonen im Kern und 6 Neutronen. Wenn man nun zwei weitere Neutronen in den Kern packt, bleibt das ganze immer noch Kohlenstoff, weil die chemischen Eigenschaften von den Protonen abhängen. Mit den beiden zusätzlichen Neutronen ist der Kern jetzt aber quasi unausgewogen und hält nicht mehr zusammen. Diese Varianten des Kohlenstoffs mit der Bezeichnung C14 ist also radioaktiv.
Auch von Technetium existieren verschiedene Isotope. Hier ist aber jedes radioaktiv, es gibt also keine Variante des Technetiumatoms die dauerhaft stabil ist. Manche zerfallen schon nach wenigen Stunden, manche brauchen mehr als 4 Millionen Jahre. Aber kein Technetiumatom überlebt ewig. Auch das wäre aber noch kein Grund, es nicht nachweisen zu können. Auch andere Elemente besitzen keine stabilen Isotope; Radium zum Beispiel, das chemische Element das von Marie und Pierre Curie entdeckt wurde und mit dem man die ganze Sache mit der Radioaktivität erst so richtig verstanden hatte, wie ich in Folge 126 erzählt habe. Radium zerfällt noch viel schneller; da ist schon nach ein paar 1000 Jahren quasi alles zerfallen. Dass die beiden Curies es trotzdem entdecken konnten liegt daran, dass es von der Natur immer wieder neu produziert wird. Und zwar dann, wenn andere radioaktive Atome zerfallen. Uran zum Beispiel, das ebenfalls radioaktiv ist und wenn es dann zerfällt, tut es dann unter anderem zu Radium. Und weil Uran zwar instabil ist, aber WIRKLICH lange braucht um zu zerfallen, ist heute immer noch genug Uran da, das zu Radium zerfallen kann, das man dann nachweisen kann.
Bei Technetium funktioniert das nicht. Es gibt zwar radioaktive Prozesse bei denen es entstehen kann, aber das tut es nur in verschwindend geringen Mengen. Und weil es selbst auch wieder nach kurzer – zumindest wenn man es nach geologischen Maßstäben misst – Zeit zerfällt, kommt es in der Erde quasi nicht vor. Selbst wenn bei der Entstehung des Planeten vor 4,5 Milliarden Jahren Technetium vorhanden gewesen wäre – was nicht der Fall war, wie ich gleich noch erklären werde – wäre heute nichts mehr davon übrig. Das Technetium das wir heute auf der Erde haben und deswegen auch erforschen können, stammt aus den radioaktiven Rückständen von Kernwaffentests oder wurde künstlich hergestellt.

Warum aber erzähle ich in einer Folge der Sternengeschichten etwas über ein chemisches Element, dass zwar sehr interessant ist, aber quasi nicht existiert und nur künstlich hergestellt werden kann. Weil es eben DOCH auch anders produziert werden kann als von Menschen im Labor! Im Jahr 1952 veröffentlichte der amerikanische Astronom Paul Merril einen Artikel mit dem eher unscheinbaren Titel „Spektroskopische Untersuchung von Sternen der S-Klasse“. Und damit war nicht die Kühlerfigur eines Mercedes gemeint, es ging um Sterne am Ende ihres Lebens, sogenannte rote Riesen. Die hat Merril spektroskopisch untersucht, das heißt er hat das Licht der Sterne in seine Bestandteile aufgespalten und daraus die chemische Zusammensetzung der Sterne bestimmt. Ich hab das Prinzip ja schon oft erklärt: Wenn Licht aus dem Inneren eines Sterns nach außen strahlt, kann es von den Atomen blockiert werden. Jedes chemische Element stoppt Licht bei ganz bestimmten Wellenlängen und wenn man dann im Licht nachsieht, wo etwas fehlt, weiß man, welche chemischen Elemente im Stern vorhanden sein müssen. Das war natürlich jetzt nur eine sehr vereinfachte Erklärung der Spektroskopie. Aber es geht jetzt auch nicht um die Technik, sondern um das Resultat. Dass was Merril in den roten Riesensternen gefunden hat war nämlich – Überraschung! – Technetium.
Was man durchaus als Sensation bezeichnen kann. Denn was bedeutet das? Technetium überlebt nur ein paar Millionen Jahre und kommt von selbst in der Natur nicht vor. Wenn es jetzt also in Sternen zu finden ist, dann bleiben nur zwei Möglichkeiten. Erstens: Das Universum ist nur ein paar Millionen Jahre alt und bei seiner Entstehung sind gleichzeitig auch alle Elemente entstanden, inklusive Technetium. Das bisschen, das vom Anfang noch übrig ist, finden wir jetzt noch in den Sternen. Das ist aber eher unwahrscheinlich. Erstens war auch 1952 schon klar, dass das Universum auf jeden Fall einige Milliarden Jahre alt ist und nicht nur ein paar Millionen. Und wenn Technetium tatsächlich beim Urknall mit allen anderen Elementen entstanden ist und ein Teil davon bis heute überdauert hat, dann müsste man ja auch auf der Erde noch etwas davon finden.
Bleibt Möglichkeit zwei: Technetium wird im Inneren von Sternen immer wieder nachproduziert. Diese Idee war zu Beginn der 1950er Jahre zwar nicht völlig neu, aber auf jeden Fall noch sehr frisch. Ursprünglich ging man nämlich tatsächlich davon aus, dass alle chemischen Elemente direkt beim Urknall selbst entstanden sind. Aber es gab immer mehr Hinweise darauf, dass das nicht der Fall war. Und dass beim Urknall selbst nur Wasserstoff und Helium, die beiden simpelsten Elemente mit den einfachsten Atomkernen gebildet worden sind. Der ganze Rest musste anderswo her kommen und das konnten nur die Sterne sein. In deren Inneren herrschen enorm hohe Temperaturen; so hoch, dass Atomkerne dort fusionieren können um neue, schwerere Atomkerne zu bilden. Was fehlte war einerseits eine stimmige und funktionierende Beschreibung WIE genau das passieren soll. Also welche Atome unter welchen Bedingungen zu welchen anderen Atomen fusionieren können, und so weiter. Es fehlte quasi das Kochrezept mit dem erklärt werden konnte, wie man aus Helium und Wasserstoff den ganzen Rest des Periodensystems basteln kann. Was außerdem fehlte war ein einwandfreier Beweis dafür, dass die Elemente WIRKLICH im Inneren der Sterne durch Kernfusion entstehen.
Diesen Beweis lieferte Merril mit seinem Nachweis von Technetium bei roten Riesensternen. Und das Kochrezept lies dann auch nicht mehr lange auf sich warten. 1957 veröffentlichten Margaret Burbidge, Geoffrey Burbidge, William Fowler und Fred Hoyle einen Fachartikel in dem sie genau das erklärten. Mit dem heutigen Stand des Wissens läuft die Entstehung von Technetium, vereinfacht gesagt, so ab. Zuerst läuft in einem Stern wie unserer Sonne tatsächlich nur die normale Fusion von Wasserstoff zu Helium ab. Irgendwann ist der Wasserstoff aber verbraucht und der Stern fängt an, das Helium zu fusionieren, zum Beispiel zu Kohlenstoff oder Sauerstoff. Das macht er bei viel höheren Temperaturen, weswegen er sich auch ausdehnt. Er wird zu einem roten-Riesenstern. Eine bestimmte Art dieser Riesensterne heißt „AGB-Sterne“ und ich werde sie sicher mal in einer eigenen Folge genauer vorstellen. Für jetzt reicht es zu wissen, dass diese Sterne quasi aus Schalen bestehen. Im Kern selbst wird kein Wasserstoff oder Helium fusioniert, dort werden nur noch die schwereren Elemente verbrannt. Weiter außen aber gibt es Schalen, in denen weiterhin Wasserstoff zu Helium oder Helium zu Kohlenstoff wird. Kurz gesagt: Überall im Stern laufen unterschiedliche nukleare Fusionsreaktionen ab. Bei manchen dieser Reaktionen werden Neutronen frei und bewegen sich durch den Stern hindurch. Die können von anderen Atomkernen eingefangen werden; diese Atomkerne werden durch die zusätzlichen Neutronen schwerer und manchmal instabil, also radioaktiv. Sie zerfallen dann und eines der Elemente das bei diesen Zerfallsreaktionen entstehen ist Technetium.

So schaffen es rote Riesensterne das Technetium herzustellen. Damit es dann aber auch im Licht der Sterne nachweisbar ist, muss es aus dem Inneren in die äußeren Schichten transportiert werden, aus denen das Sternenlicht hinaus ins All gelangt. Das passiert nur in speziellen, sehr kurzen Lebensphasen eines Riesensterns, immer dann wenn bestimmte Fusionsreaktionen starten oder zu Ende gehen. Zum Beispiel dann, wenn ein Stern anfängt Helium zu fusionieren – oder diese Fusionsphase in einer Schale endet. Dann ändern sich die Temperaturen im Stern und sein Material kann durchgemischt werden. Zeug das eigentlich immer tief unten im Stern war kann dann noch oben steigen; Material von oben kann nach unten in den Stern sinken. So gelangt auch das Technetium nach oben, wo Merril – und seitdem jede Menge andere – es nachweisen konnten. Irgendwann endet dann das Leben des Sterns selbst, die Fusion kommt zum Erliegen und er schleudert seine ganzen verbliebenen Gasschichten hinaus ins All. Dort verteilen sich all die neu geschaffenen chemischen Elemente und wenn dann neue Sterne entstehen oder Planeten, haben die schon eine Grundausstattung schwerer Elemente. Bis auf Technetium. Das ist nämlich schon wieder längst zerfallen, wenn dieser Prozess stattfindet. Es existiert wirklich nur im Inneren dieser roten Riesensterne. Man findet es nur im Himmel und nicht hier unten auf der Erde. Trotzdem können wir es beobachten und daraus lernen, wie die Sterne am Himmel funktionieren. Es ist ein wahrhaft astronomisches Element.
Irdisches Technetium wird mittlerweile gezielt hergestellt. Dazu nimmt man stabiles Molybdän (Mo-98) und setzt es Neutronenstrahlung aus. Es entsteht ein gewisser Anteil von Mo-99 mit einer Halbwertszeit von 66 Stunden. Vor Ort, in einer radiologischen Praxis oder Klinik, wird das Tochternuklid Tc-99m abgetrennt und etwa bei einer Schilddrüsenszintigrafie verwendet.
Wenn dieses Kernisomer per Isomerieübergang zu TC-99 zerfällt, zeichnet ein Scanner die Gammastrahlung auf, die aus dem Körper des Patienten kommt, und generiert daraus ein Bild. Das entstehende TC-99 zerfällt in geologischer wie astronomischer Sicht ziemlich schnell. Bei einer Halbwertszeit von 211.100 Jahren dauert es natürlich trotzdem eine ganze Zeitlang, bis es wieder von der Erde verschwunden sein wird. Es kann allerdings auch per Betazerfall zu stabilem Ru-99 werden, was aber vermutlich für die Untersuchung eher unerwünscht ist.
Die benachbarten Elemente Molybdän und Ruthenium haben sehr viele stabile Isotope und es bestätigt sich die Mattauchsche Isobarenregel, nach der Elemente mit ungerader Ordnungszahl und Nachbarelementen mit vielen stabilen Isotopen instabil sind. Das ist ein kernphysikalischer Effekt, der wie so viele nicht anschaulich nachzuvollziehen ist.
1961 wurde übrigens in 5,3 kg Pechblende aus Katanga tatsächlich ein Nanogramm Technetium nachgewiesen. Das muss dann ohne menschliches Zutun aus dem Uran entstanden sein.
Schade, jetzt muss ich meinen üblichen Kommentar zu der Werbeaussage „enthält nur100% natürliche Inhaltstoffe“: „Aha, da ist kein Tc enthalten.“ überdenken.
Hat man bis jetzt kein stabiles TC-Isotop gefunden, oder ist es aus physikalischen Gründen nicht möglich, dass ein stabiles Nuklid existiert ?.
Hmm. Ich erkenne keinerlei Chemie in dem Artikel – und erst recht nicht am Anfang.
Allerhöchstens noch in der Zwiebel – aber die ist eher Biologie.
Eigentlich erkenne ich nur Physik – zumeist Kernphysik.
Kann mich mal einer Erleuchten, auf welche Teile des Artikels sich Florian mit „Chemie“ bezieht?
🙂 🙂
@Ludwig: Es geht um ein chemisches Element. Wenn du darauf hinweisen willst, dass die Grenzen zwischen Chemie und Kernphysik fließend sind… ich glaube, das kann man als gegeben ansehen.
AGB-Sterne?
Kenn ich nur aus der Werrbung…
Sehr interessant, viel gelernt.
Wäre es möglich, dass du zu jedem Element solch einen Blog machst, Florian?
Technetium war der gesuchte Begriff des Astrodictum-Simplex-Sommerrätsels des Jahres 2017. Damals haben wir uns schon einmal mit diesem Element beschäftigt und es hat auch einige Zeit und Aufwand benötigt, um es zu finden.
Ich freue mich schon auf das diesjährige Rätsel.
Technetium, hatte ich vorher nie wirklich auf dem Schirm. Da weiß ich mal wieder, warum ich jede der 396 Folgen Sternengeschichten gehört habe. Man lernt halt immer wieder etwas dazu.
@Florian Freistetter: Ich könnte jeden Tag eine Folge hören.
@bote: Elemente mit Ungerader Ordnungszahl tendieren instabiler zu sein, also solche mit gerader Ordnungszahl (das ungerade Teilchen was übrig bleibt, ist „lockerer“ gebunden). Mit der Bethe-Weizsäcker-Formel kann die Bindungsenergie berechnet werden, da gibt es einen Symmetrie Anteil, der verschwindet für N = Z, für alle anderen Konstellationen verringert er E_B. Tc hat zwar einige langlebige Isotope (mehrere Millionen Jahre), aber keines welches als stabil gelten kann.
Mit der empirisch gefundenen (Mattauchsche) Isobarenregel kann man dies auch erklären, da diese Regel verlestzt werden würde, wenn es neben den vielen stabilen Isotopen von Molybdän und Ruthenium auch stabile Tc Isotope geben würde.
Moment, ich dachte in Sternen können nur Elemente bis zum Eisen produziert werden, alle schwereren nur in Supernovaen, wie kann da jetzt das viel schwerere TC (bzw noch Schwerere die dann wieder zu TC zerfallen) in einer Schale eines Sterns entstehen?
@Max
Technetium entsteht durch den s-Prozess in so genannten AGB-Sternen (Asymptotic Giant Branch). Das sind Riesensterne, die so schwer sind wie mehrere Sonnen. Diese Sterne haben einen ungewöhnlichen Aufbau: Sie haben ein inaktives Zentrum, um das zwei dünne Schalen aus Wasserstoff und Helium angeordnet sind und wo abwechselnd Kernfusion stattfindet. Weiter außen befindet sich eine dicke Wasserstoff-Hülle. In einer Übergangszone zwischen den beiden Hüllen werden langsame Neutronen erzeugt, die von Atomkernen eingefangen werden können. Dabei entstehen schwerere Elemente wie zum Beispiel Technetium.
Guter Artikel!
Ich liebe ja die radioaktiven Elemente.
Wieder was dazugelernt.
Das erinnert mich an Doktor Plichta und seine Zahlenmystik, die er um das nicht existierende Technetium entfachte. Überflieger erkannten Plichtas Zauberkünste unschwer als Mumpitz, ich allerdings hielt das als junger Mensch durchaus für glaubhaft.
Indes war die Lektüre nicht ganz umsonst, denn Plichta wusste über ein zweites leichtes und unstabiles Element zu berichten: das Promethium mit Ordnungszahl 61. Wäre das nicht auch interessant?
@Artur57
Oh der Peter Plichta. Ein bunder Hund. 🙂
Hallo Florian
ich habe begonnen deine Sternengeschichten zu hören und wurde bereits in ihren Bann gezogen 🙂
Danke vielmals für deinen Einsatz und die spannenden Podcasts.